不丹防护用品市场准入
2020-04-28 09:14(一)监管机构
成立于2004年6月的不丹药品监督管理局(Drug Regulatory Authority, DRA)是不丹卫生部下属的监管药品和医疗器械进口和销售的重要部门。在制定政策法令方面,不丹药监局直接向不丹药品委员会(Bhutan Medicines Board)报告。药品技术顾问委员会(Drug Technical Advisory Committee, DTAC)和血液技术顾问委员会(Blood Technical Advisory Committee ,BTAC)为药监局提供技术支持。药监局下辖三个技术部,注册部,检查部,市场监管部,这三个部门的工作由管理部和财务部支持。

图1 不丹药品监督管理局组织架构
不丹药监局的主要职能:
授权制造,进口,出口,销售,分销和储存包括血液和血液制品在内的药品。
负责国内生产或进口到该国的药品注册。
监管从事药品进口,储存,制造和销售的人员的能力和技能。
对生产,销售,分销和储存包括血液和血液制品在内的医药产品的场所进行检查/监管。
以不丹国家配方和药物安全信息的形式提供最新信息。
监测由药品引起的不良反应的趋势和情况。
向公众介绍药品的使用和有害作用。
促进政策,以改善对具有成本效益的优质药品的获取。
对与药品有关的问题进行研究。
以经济有效的方式向公众提供监管服务。
(二)法律法规
现阶段不丹还没有明确的医疗器械法规来监管产品的安全、质量和性能。根据不丹药品委员会(Bhutan Medicines Board)的指示,不丹药监局正在制定医疗器械法规(Medical Device Regulation).
根据不丹药品监管局(Drug Regulatory Authority,DRA) 2018年6月发布的Medical Device Control Strategy 2018-2023, 2019年6月,DRA打算制定并出台一份医疗器械法规(Medical Device Regulation,MDR)。实际情况是截至2020年3月份至今还未出台。不过在MDR法规发布之前,不丹药监局将采用全球医疗器械协调工作组(GHTF)制定的标准,以及后来的国际医疗器械监管者论坛(IMDRF)制定的医疗器械标准。
根据正在制定的医疗器械法令(MDR),不丹药监局打算将医疗器械按风险由低到高分为A类、B类、C类、D类共四级。例如测温仪属于A类,心脏起搏器属于D类,不过未说明防疫产品属于哪一类。A类产品不需要注册,主要通过进口授权和上市后监管。B类,C类,D类需要注册,也通过进口授权和上市后监管。
现有药品相关的监管法令如下:
药品法案,2003
不丹药品法规法令2019
国家药品政策2007
不丹血液及血液制品法令2016
(三)清关流程和材料
在不丹,注册证书和进口许可证是进口药品和医疗器械的强制性要求。
注册证书:要注册药品,首先当地经销商(称为市场授权持有人Market Authorization Holder)或制造商应向DRA申请销售和分销技术授权(Technical Authorization for Sale and Distribution),经济事务部下属的贸易司将根据该授权签发商业许可证(Trade License)。获得销售和分销的商业许可证和技术授权后,当地经销商可以将与药品有关的文件提交DRA进行注册。 如果不丹以外的制造商希望直接注册药品,也可以这样做。如果相关资料准备充分,大约1-3个月时间可以完成,注册证书有3年有效期。
如果药品在如下国家药品监管机构完成了注册,进入不丹可以免除注册:澳大利亚的TGA, 加拿大的HC, 美国FDA, 欧盟EMA, 英国MHRA, 日本DRA,新加坡HSA,马来西亚BPFK,泰国FDA.或是由WHO,UN, OIE或其它联合国机构预认证过的药品及疫苗。
进口许可证:药品与医疗器械在不丹属于进口管制产品,进口的时候需要获得药监局颁发的进口授权(Import Authorization)。进口授权只能颁发给市场授权持有人(market authorization holder),不丹当地注册的药店,政府采购部门,国际组织或是由药监局DRA授权的个人。
不丹主管进口的部门为经济贸易部(Ministry of Economic Affairs)下属的贸易司(Department of Trade)。在不丹,获得注册证书和进口许可证是进口药品和医疗器械的强制性要求。
在进口产品到达不丹之前,进口商或是其授权代理人需向位于印度加尔各答的不丹海关联络中转办公室( the Bhutanese Revenue and Customs Liaison and Transit Office)提交如下资料:
1. 进口许可证副本;
2. 海运提单/空运提单/装船清单,需由进口商和相关银行盖章;
3. 发票;
4. 装箱单
5. 原产地证
6. 海运保险/空运保险/陆运保险
货物到达不丹7个工作日内,进口商或是其授权代理商应完成清关手续。清关时,进口商或是其授权代理商需提交进口声明表,主要包含内容如下:
1. 进口声明表应包括进口产品的详细信息,进口商需保证其真实性,并附上货运单据及银行盖章的发票。
2. 如果有必要,海关官员应该对进口产品进行实物检查。
3. 如果海关官员检查产品没有问题,在进口商交付了关税、销售税及其它费用之后,就应该发出放行指令。
(四)相关标准
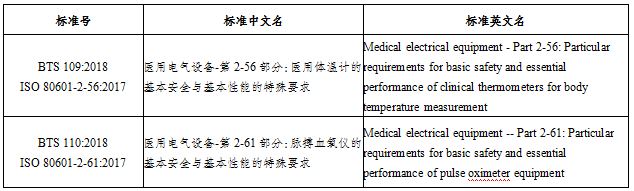
不丹卫生部下辖的医疗用品和卫生基础设施部(Department of Medical Supplies and Health Infrastructure,DoMSHI)下设的生物医学工程处(Bio-Medical Engineering Division,BMED)采用了50多项医用电气设备IEC和ISO标准做为国家标准。与防疫相关的标准涉及医用体温计及脉搏血氧仪标准,这两个标准等同采用了ISO标准,具体情况如下表2。不过不丹标准局(Bhutan Standards Bureau)也在与相关利益方合作制定本国的医疗器械标准。
不丹药监局可接受的标准有:国际标准(WHO,ISO,IEC,GHTF,IMDRF等)、印度BIS标准、欧美主要发达国家(FDA等)。目前,不丹政府不接受中国标准(包括国家标准、行业标准、企业标准等)。
表1:不丹防疫产品标准(等同采用ISO标准)
成都市标准化研究院 编辑